SEHAT ITU MURAH | Liong Pit Lin
Berita besar, D-Kawan: insulin yang tidak dapat bertindak pantas yang dikenali sebagai Afrezza baru saja mendapat kelulusan FDA!
Ketiga kalinya pesona untuk penggubalan insulin yang tidak dapat dirahsiakan ini, yang kedua kemudian membuatnya melalui proses pengawalseliaan U. S. selepas Pfizer gagal gagal menjadi Exubera yang lebih baik satu dekad yang lalu.
Pada hari Jumaat, syarikat bioteknologi California, MannKind Corp akhirnya memperoleh kelulusan peraturan untuk peranti Afrezzanya.

Sekarang, selepas menyerahkan semula Afrezza pada bulan Oktober 2013, MannKind akhirnya meyakinkan FDA bahawa ia bersedia untuk masuk ke tangan orang dewasa dengan diabetes!
Kami diberitahu oleh eksekutif utama MannKind bahawa mereka sedang berusaha untuk mencari rakan kongsi farmasi untuk menghasilkan dan mengedarkan Afrezza, dan produk itu boleh disediakan secepat Januari, atau akhir suku pertama 2015. > Dalam siaran berita FDA yang dikeluarkan pada hari Jumaat, Dr. Jean-Marc Guettier dari Bahagian Metabolisme dan Produk Endokrinologi, menyatakan: "Kelulusan hari ini memperluaskan pilihan yang tersedia untuk menyampaikan insulin pada waktu makan dalam pengurusan keseluruhan pesakit diabetes yang memerlukannya untuk mengawal paras gula darah. "
Afrezza adalah insulin ultralasid yang bertindak dalam bentuk serbuk yang direka sebagai insulin pra-makanan untuk orang dewasa (belum lagi untuk kanak-kanak ) dengan diabetes jenis 1 atau jenis 2. Ia bertujuan untuk pancang gula darah selepas makan, yang bermaksud digunakan dengan rawatan insulin yang sedia ada dan tidak dimaksudkan sebagai rawatan insulin yang berdiri sendiri.
Insulin serbuk dikendalikan melalui inhaler bersaiz whistle yang dipanggil Dreamboat, yang dibangunkan selepas pusingan pertama FDA dan menyebabkan kelewatan kerana agensi itu mahukan lebih banyak kajian klinikal menggunakan inhaler baru itu. Serbuk itu segera larut apabila disedut ke dalam paru-paru, dan insulin kemudiannya dibuang ke dalam aliran darah untuk mula bekerja. Afrezza puncak dalam masa 12 hingga 15 minit dan keluar dari sistem dalam masa sejam, berbanding dengan insulin jangka pendek semasa yang biasanya mengambil masa sekurang-kurangnya 20 minit untuk menendang, puncak pada 2-3 jam, dan boleh tinggal di dalam sistem untuk selama lima jam.
Sudah tentu, rayuan terbesar adalah bahawa ia tidak memerlukan jarum, tetapi hanya sedikit inhaler tangan yang benar-benar kelihatan seperti wisel.Dreamboat dimaksudkan untuk dibuang selepas 15 hari untuk mengelakkan sebarang pembentukan serbuk di dalam yang boleh menyumbat peranti. Tidak seperti insulin tradisional, ia tidak memerlukan penyejukan, tetapi disimpan pada suhu bilik. Setiap kartrij satu guna akan memegang sama ada 4 atau 8 unit, dan pada masa Afrezza dikomersialkan, terdapat 12 unit kartrij yang tersedia.
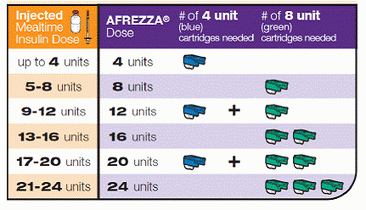
Berikut adalah cara anda boleh membuatnya, menukar jumlah suntikan insulin atau bolus ke dalam minuman beralkohol yang mesra Afrezza:
Secara peribadi, itu tidak kelihatan seperti banyak insulin untuk menampung beberapa makanan yang saya makan memerlukan dos yang lebih tinggi … saya akan melalui sekumpulan kartrij kecil itu. Jadi bagi sesetengah OKU, peranti ini mungkin menimbulkan cabaran logistik dari segi dengan mudah menampung jumlah yang kita perlukan …? Tetapi sekali lagi, ini mungkin alat yang baik untuk mengetuk gula darah yang keras kepala dengan dos pembetulan.
Dalam perbualan telefon lewat Jumaat, presiden MannKind, Hakan Edstrom memberitahu kami syarikat itu belum memuktamadkan apa-apa perjanjian dengan bakal calon untuk mengilang dan mengedarkan Afrezza. Tetapi semakin dekat, dan dalam perbincangan dengan beberapa syarikat untuk memuktamadkan perkongsian secepat mungkin.
Kos tetap TBD (banyak bergantung kepada perkongsian berpotensi), tetapi Edstrom mengatakan mereka menjangkakan harga berada dalam lingkungan yang sama seperti yang kami bayar pesakit sekarang untuk pen insulin di ASKelulusan ini adalah pembangunan BESAR, dan telah lama datang, lapan tahun sejak usaha ini dimulakan oleh Alfred Mann - orang yang mengasaskan Minimed sebelum akhirnya dibeli oleh Medtronic. Kami telah mengikuti kisah Afrezza selama bertahun-tahun di sini di ' Mine
- dari hari-hari pemfailan FDA awal apabila MannKind mempunyai reka bentuk klausa awalnya, untuk liputan yang lebih baru mengenai bagaimana Afrezza digunakan dalam Pankreas Buatan ujian klinikal.
Semua itu berkata, ia masih agak mengejutkan bahawa Afrezza mendapat kelulusan FDA, memandangkan kajian semula staf agensi itu telah membangkitkan tentang keselamatan dan keberkesanan produk. Terdapat kebimbangan awal bahawa pendedahan jangka panjang paru-paru kepada insulin boleh menyebabkan kanser paru-paru, kerana data percubaan klinikal menunjukkan lebih banyak kes kanser paru-paru di kalangan mereka yang menerima Afrezza daripada yang lain dalam kumpulan kawalan. Tetapi bilangannya adalah kecil dan jauh dari definitif, dan MannKind dikehendaki menjalankan kajian jangka panjang untuk menilai risiko itu.
Jawatankuasa penasihat yang bertemu pada 1 April tahun ini mengundi 13 hingga 1 bahawa Afrezza adalah selamat dan cukup berkesan untuk mendapat kelulusan sebagai rawatan untuk diabetes jenis 1, dengan penyokong tunggal David Cooke mengundi bahawa risiko melebihi manfaat untuk jenis 1s.Beliau menunjuk kepada kajian FDA dalaman yang menunjukkan beberapa pesakit yang mengambil Afrezza menghentikan rawatan selepas mengalami kekejangan bronkial, batuk, dan penurunan dalam fungsi paru-paru mereka. Tetapi tidak ada kebimbangan yang timbul semasa pengundian pada Afrezza untuk kegunaan jenis 2, dan jawatankuasa itu memutuskan sebulat suara memihak kepada undi 14-0.
Dalam meluluskan Afrezza, FDA telah melampirkan beberapa keselamatan, keberkesanan dan keperluan penggunaan pesakit:Ia tidak disyorkan untuk orang yang menghidap kencing manis atau juga untuk mengobati ketoasidosis diabetes (DKA).

FDA memerlukan Amaran Berkotak, menasihatkan bahawa sesetengah orang yang mempunyai penyakit paru-paru dan kronik paru-paru (COPD) yang telah menggunakan Afrezza telah mengalami bronchospasm akut. Akibatnya, mereka yang mengalami penyakit paru-paru kronik, asma atau COPD, tidak harus menggunakan Afrezza kerana risiko ini. Reaksi yang paling biasa yang berkaitan dengan Afrezza dalam ujian klinikal adalah hipoglikemia, batuk, dan sakit tekak atau kerengsaan.
Sebahagian daripada keperluan kelulusan adalah Strategi Penilaian Risiko dan Mitigasi, yang mesti termasuk rancangan komunikasi untuk memberitahu profesional penjagaan kesihatan tentang risiko serius bronkospasm akut yang dikaitkan dengan Afrezza. Ini bermakna untuk memastikan bahawa manfaat lebih besar daripada potensi risiko menggunakan Afrezza.
- Kajian pasca pasaran lain diperlukan pada Afrezza, seperti: percubaan klinikal untuk menilai potensi risiko keganasan paru dengan penggunaan (percubaan ini juga akan menilai risiko kardiovaskular dan kesan jangka panjang Afrezza pada fungsi paru-paru); dan dua percubaan klinik glukosa-klac farmakokinetik-pharmacodynamic, satu untuk mencirikan tindak balas dos dan satu untuk mencirikan kepelbagaian dalam-subjek.
- Edstrom memberitahu kami mereka merancang untuk memulakan percubaan pediatrik secepat mungkin, yang secara realistik akan bermula pada pertengahan 2015. Ini bermakna Afrezza mungkin tidak diluluskan untuk kanak-kanak yang menghidap diabetes sehingga 2017, dan proses pengawalseliaan itu mungkin berbeza-beza bergantung kepada apa yang ditunjukkan oleh kajian pasca pasaran dan penggunaan dewasa menggunakannya.
- Dan walaupun cahaya hijau FDA, tidak ada jaminan Afrezza akan melihat kejayaan komersil atau orang-orang OKU akan berduyun-duyun untuk menggunakannya. Seperti yang dinyatakan, MannKind belum memperoleh mana-mana rakan kongsi farmasi bersedia untuk menjual Afrezza. Tetapi jika pendapatan MannKind memanggil pada bulan Mei adalah apa-apa petunjuk mengenai apa yang akan berlaku tidak lama lagi, perkongsian berpotensi mungkin tidak jauh.
- Dari sudut pandangan pelabur, ramai yang ragu-ragu berdasarkan insulin yang terhidu Exubera yang gagal yang telah banyak membincangkan mengenai Afrezza sejak beberapa tahun yang lalu. Produk bersama Pfizer-Sanofi ini ditarik dari pasaran pada tahun 2007 selepas lebih daripada jualan subpar bernilai setahun - menghasilkan rekod $ 2. 8 bilion kerugian untuk vendor.
- Sudah tentu, MannKind mendakwa bahawa Afrezza sangat berbeza, terutamanya kerana Exubera menggunakan inhaler kaki panjang dan dikaitkan dengan risiko kanser paru-paru yang lebih tinggi yang tidak dapat diatasi Pfizer.
Kita akan lihat apa yang D-Komuniti fikir sekarang dengan Afrezza, terutamanya dengan semua perhatian percubaan klinikal AP yang baru-baru ini. Sama ada cukup untuk meyakinkan orang ramai masih belum jelas …
Mulakan berita sekarang, dan kita akan melihat berapa lama masa yang diperlukan bagi kita semua untuk menghembus nafas dan menjadikan keghairahan ini menjadi jualan sebenar dan penggunaan yang meluas.
Penafian
: Kandungan yang dicipta oleh pasukan Diabetes Mine. Untuk butiran lanjut klik di sini.
Penafian
Kandungan ini dibuat untuk Diabetes Mine, blog kesihatan pengguna yang memberi tumpuan kepada komuniti diabetes. Kandungan tidak disemak secara medis dan tidak mematuhi garis panduan editorial Healthline. Untuk maklumat lanjut mengenai perkongsian Healthline dengan Diabetes Mine, sila klik di sini.
Diabetes Berita: Dexcom SHARE Dapat Kelulusan FDA!

Sistem Bluetooth Dexcom SHARE wayarles telah diberikan meneruskan FDA. Dexcom SHARE membolehkan data dari CGM anda dihantar ke telefon pintar anda.
Inhaled Insulin Afrezza Telah Diberi Kelulusan FDA

FDA meluluskan produk insulin yang terhirup yang baru. Afrezza adalah insulin ultrarapid yang bertindak dalam bentuk serbuk, yang direka sebagai hidangan pra untuk pesakit kencing manis jenis 1.
Kelulusan FDA: Baik, Buruk, atau Hanya Hilang?


